文献进展
文献进展
核苷和核苷酸类药物治疗慢性乙型肝炎的长期性源自:中华肝脏病杂志
近20年来,临床和流行病学研究表明,持续、活跃的HBV复制是慢性乙型肝炎(CHB)疾病进展的最重要因素,只有长期抑制HBV复制,才有可能防止疾病进展。但HBV在复制过程中,在肝细胞核内形成共价闭合环状DNA (covalently closed circular DNA, cccDNA)并可持续存在;核苷和核苷酸类药物(nucleoside and nucleotide analogs,NAs)主要抑制HBV复制的逆转录环节,对cccDNA无直接抑制或清除作用;CHB患者存在特异性免疫功能障碍,而NAs无直接的免疫调节作用。
因此,现有NAs抗病毒治疗很难彻底清除HBV,仅部分HBeAg阳性并伴有明显ALT升高的患者可实现HBeAg血清学转换,甚至HBsAg消失或HBsAg血清学转换,而大部分CHB患者,尤其是HBeAg阴性CHB和肝硬化患者,需要长期抗病毒治疗。因此,目前国内外CHB管理共识或指南均将治疗目标确定为:最大限度地长期抑制HBV复制,减轻肝细胞炎症坏死和纤维化,延缓和减少肝脏失代偿、肝硬化、肝细胞癌(HCC)及其并发症的发生,从而改善生活质量和延长存活时间。
为帮助临床医生正确认识NAs治疗的长期性,合理选择抗病毒药物、系统监测其疗效和不良事件并长期随访其临床转归,国内部分肝脏病学和感染病学专家根据国内外最新研究证据,经过认真讨论和反复修改,最终形成本文。
一、NAs长期治疗的必要性
1.病毒因素:HBV复制过程可分6个环节:(1)病毒进入肝细胞浆,其核衣壳被裂解而形成松弛型环状DNA(relaxed circular DNA,rcDNA),后者进入肝细胞核,并在病毒DNA聚合酶和宿主酶的作用下,修复rcDNA成为cccDNA;(2)以cccDNA为模板,在宿主细胞RNA聚合酶作用下,转录成4种不同长度的病毒mRNA和前基因组RNA(pgRNA),翻译HBV的各种蛋白;
(3)病毒聚合酶和衣壳化信号共同作用于pgRNA,启动逆转录和核衣壳组装;(4)通过逆转录,合成病毒负链DNA,同时病毒聚合酶消化病毒RNA模板;(5)病毒负链DNA合成后,剩余的RNA作为引物,启动正链DNA合成;(6)完成正链DNA合成,形成rcDNA,同时核衣壳被包被上外膜并作为感染性病毒体分泌至细胞外;或再回到同一个肝细胞核内,扩增或维持cccDNA库(图1)。
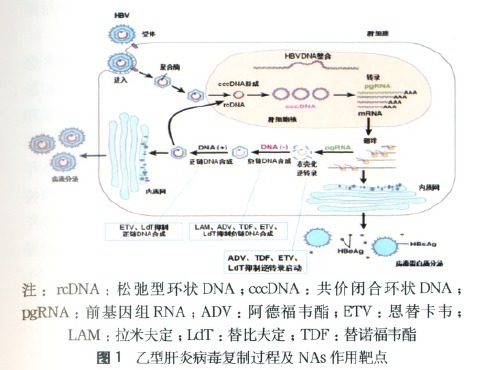
现有的NAs只作用于HBV复制的(3)、(4)、(5)环节,对病毒复制的其他环节无明显作用。因此,cccDNA可在肝细胞内持续存在并作为HBV的复制模板,持续产生子代HBV,感染其他肝细胞。
cccDNA 一旦在肝细胞核内形成,即具有高度稳定性,可持续产生子代病毒而不受细胞分裂的影响。据数学模型推算,应用阿德福韦酯(adefovir dipivoxil tablets,ADV)治疗的患者,需要14.5年才能完全清除其肝细胞核中的cccDNA。因此,尽管NAs治疗可有效抑制HBV复制,少数患者可达到HBeAg血清学转换甚至HBsAg消失,但肝细胞核内仍可能残存cccDNA,停药后仍有可能复发。
2.药物因素:NAs在细胞内经磷酸化后,生成三磷酸核苷活性产物,通过竞争抑制作用,阻止内源性核苷酸参与HBV DNA的复制,快速有效地减少HBV DNA的合成。有研究表明,ADV、替诺福韦酯(tenofovir disoproxil fuma rate,TDF)、恩替卡韦(entecavir,ETV)和替比夫定(telbivudine,LdT)可抑制逆转录启动;拉米夫定(lamivudine,LAM)、ADV、TDF、ETV和LdT可抑制病毒负链DNA合成;ETV和LdT可抑制正链DNA合成(图1)。
但对HBV复制的中间产物cccDNA不起作用,因此,NAs不能清除在治疗前已存在的,或在治疗过程中因未完全抑制HBV复制而新产生的cccDNA。
此外,cccDNA、HBeAg和HBsAg的减少或清除主要依赖于宿主免疫系统的作用。NAs可暂时改善机体对HBV的免疫应答,但无直接免疫调节作用。尽管NAs可有效降低肝细胞和血清中HBV DNA水平,但对血清中HBeAg和HBsAg水平无明显降低作用。因此,NAs有限疗程治疗难以达到停药后持久的免疫应答。
3.宿主因素:慢性HBV感染是一个长期的发展过程。在我国,接受NAs治疗的CHB患者中,大部分是在婴幼儿时期感染HBV,其病程较长,一般肝组织学均表现有不同程度的坏死炎症和肝纤维化,甚至肝硬化。但肝脏组织学改善尤其是纤维化改善需要较长的期限。Chang等随访57例经ETV治疗的HBeAg阳性或阴性患者,发现治疗48周时Ishak纤维化评分下降≥1者仅为32% (18/57),但治疗至中位时间6年(范围3-7年)时Ishak纤维化评分下降≥1者升至88% (50/57)。
4.临床实践:临床实践表明,即使按照国内外现行CHB管理共识或指南建议的标准停药,复发率仍较高(表1)。
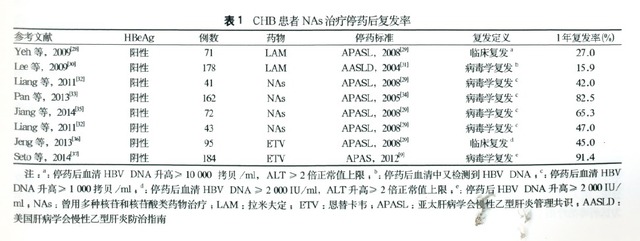
停药后复发率的高低与巩固治疗时间、判断复发的标准和停药后随访时间有关。巩固治疗时间越长,复发率越低。Jiang等报道,巩固治疗≥18个月者的复发率(15.4%)明显低于巩固治疗< 18个月者(47.5%)。
关于判断复发的标准,各家报道不一。多数报道以病毒学复发为标准,但其标准也不一致,有的以停药后血清中又检测到HBV DNA为复发;有的以停药后血清HBVDNA升高≥1 000拷贝/ml为复发;也有以停药后血清HBV DNA升高≥2 000 IU/ml为复发。
少数报道以临床复发为标准,但其标准也各异,有的以停药后血清HBVDNA升高≥10 000拷贝/ml及ALT≥2倍正常值上限为临床复发;有的以停药后血清HBV DNA≥2 000 IU/ml,ALT升高≥2倍正常值上限为临床复发。在停药标准、巩固治疗时间和随访时间相同的情况下,一般病毒学复发率高于临床复发率。
停药后随访时间越长,复发率越高。Liu等报道,停药后随访至6、12、24、36、48和60个月,累计病毒学复发率(血清HBV DNA≥10 000拷贝/ml)分别为26.2%、43.6%、49.7%、52.l%、56.1%和56.1%.
二、NAs长期治疗的临床获益
1.改善肝脏组织坏死炎症及逆转纤维化和肝硬化:应用NAs长期治疗可改善CHB患者的肝组织坏死炎症和纤维化逆转。Dienstag等用LAM治疗CHB患者,随访至中位治疗时间3.5年,56%患者肝组织坏死炎症改善,33%无改变。Xu等应用LAM治疗CHB至10年,19例患者有基线和10年时配对的肝活组织检查标本,结果21% (4/19)肝纤维化/肝硬化完全逆转,47% (9/19) Ishak评分改善,32%(6/19)肝纤维化无改善。
Hadziyannis等用ADV治疗70例HBeAg阴性CHB患者,治疗至192周或240周时,分别有86%和83%患者肝组织坏死炎症改善,73%和75%患者纤维化改善。Marcellin等用ADV治疗171例HBeAg阳性CHB患者,其中15例有基线和随访5年的配对肝活组织检查资料,67%患者肝组织坏死炎症改善,60%患者纤维化改善。
Liaw报道,641例接受TDF治疗的患者中,489例(76%)完成240周治疗,348例(54%)有基线和240周时肝活组织检查结果,该348例患者中,304例(87%)肝组织学改善,176例(51%)240周时发生肝纤维化逆转P<0.000 1);96例(28%)基线为肝硬化(Ishak评分为5或6)患者中,71例(74%)患者于240周时肝活组织检查Ishak评分下降≥1,表示肝硬化逆转。
Schiff等报道,10例进展性肝纤维化或肝硬化患者(基线Ishak评分≥4),经ETV累计治疗6年(范围267-297周),所有10例患者的肝脏组织学均改善,Ishak肝纤维化评分和Knodell肝组织坏死炎症评分较基线分别平均下降2.2和7.6分,4例基线为肝硬化患者的Ishak评分均降至4或以下。
2.逆转或缓解失代偿:一项随机非盲研究报道,195例失代偿肝硬化患者应用ETV 1 mg/d或ADV 10 mg/d治疗,48周时病毒抑制率分别为57%和20%,MELD评分下降为2.6和1.7。一项双盲研究入组112例CHB失代偿患者,随机分为TDF组(45例)、TDF和恩曲他滨(truvada)联合治疗组(45例)及ETV组(22例),治疗48周后,3组应答率相同,病毒学应答率(HBV DNA<400拷贝/ml)分别为71%、88%和73%;ALT复常率分别为57%、76%和55%;3组MELD中位评分和CTP评分下降2分及以上者的比例相同。
3.延缓或阻止肝病进展:LAM长期治疗(中位治疗时间89.9个月)142例HBeAg阳性但无肝硬化患者,其累计肝硬化发生率明显低于124例未治疗的HBeAg阳性对照组。
一项双盲随机对照研究表明,用LAM长期治疗(中位治疗时间32.4个月)436例肝硬化患者,与未治疗的215例对照组比较,治疗组和对照组的肝病进展分别为7.8%( 34/436)和17.7% (38/215),P=0.001,差异有统计学意义。VIRGIL研究报道,ETV中位治疗时间20个月(范围11-32个月)且出现病毒学应答(血清HBV DNA<80 IU/ml)的CHB患者,发生失代偿的概率下降71%。
4.预防和减少HCC的发生:多项研究报道,应用LAM长期治疗CHB患者可明显降低HCC发生率。Su等报道,666例接受ETV单药治疗肝硬化患者为ETV组,621例未接受治疗患者为对照组,在随访2.7年中,ETV组的HCC发生率为2.4%,对照组为5.2%(P=0.009),降低59%。
Wu等对中国台湾健康保险研究数据库(NHIRD)中1997年1月至2010年12月间CHB患者数据进行回顾性分析,纳入21 595例CHB患者,接受NAs治疗至少3个月,为抗病毒治疗组;另21 595例采用保肝药物治疗的患者作为对照组,结果抗病毒治疗组7年HCC发生率显著低于对照组(7.32%对比22.7%.P<0.001)。
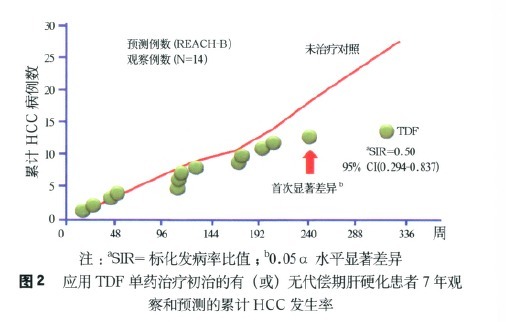
但也有一些研究报道,NAs长期治疗对CHB患者的HCC发生率无影响,这可能与研究对象不同(如患者的种族、遗传、年龄、性别、病期、基线HBV DNA和HBsAg水平、HBV基因型、CHB和肝癌家族史等构成不同)、样本量小、随访时间短等因素有关。如TDF治疗6年的注册研究报道,治疗组的HCC年发生率为0.4%,与按REACH-B评分获得的预期HCC发生率比较,最初5年TDF有效治疗对HCC发生率并无影响,但5年后两组的差异有统计学意义(图2)。
三、NAs长期治疗应注意的问题
1.初治药物选择:应用低耐药基因屏障的NAs如LAM长期治疗,可产生较高的HBV耐药突变率。发生耐药突变的患者,特别是肝硬化患者更易发生疾病进展,甚至死亡。因此,亚太、欧洲和美国肝病学会的CHB管理共识或指南均推荐,NAs初治患者应选择强效、高耐药基因屏障的药物,即ETV和TDF作为优选或一线单药治疗。我国CHB防治指南也建议:“如条件允许,初始治疗时宜选用抗病毒作用强和耐药发生率低的药物”。
2.依从性:患者对长期治疗的依从性不仅与耐药发生有关,还与抗病毒治疗的疗效有关。Hilleret等报道,用ADV治疗至2年时,依从性差的患者血清HBV DNA检测不到的患者比例明显低于依从性好的患者(21%对比42%,P< 0.01)。与依从性好的患者比较,依从性差的患者的HBeAg阳性率、血清HBV DNA载量和病毒学突破率均较高。
据调查,欧美一些国家CHB患者对NAs治疗的依从性约50%。据对我国110个城市741家医院的684例肝病相关临床医师其诊治的LAM经治CHB患者调查结果表明,自行停药换药者为47%-49%,其中治疗1年内自行停药换药者占19%-24%。叶丽华等报道,未遵医嘱用药的患者占16.7%。因此,加强对患者抗病毒治疗依从性的教育刻不容缓。
3.耐药监测:耐药是NAs长期治疗CHB所面临的主要问题之一。耐药可引发病毒学突破、生物化学突破、病毒学反弹及肝炎发作,少数患者可出现肝脏失代偿、急性肝衰竭,甚至死亡。临床试验数据表明,LAM、 ADV和ETV治疗1年耐药突变率分别为20.0%、0和0;治疗4年耐药突变率分别为64.7%. 25.7%和0.9%。ADV治疗HBeAg阳性CHB患者5年累计耐药突变率为l4.6%。LdT单药治疗104周耐药突变率为25. 8%。根据已发表的数据,TDF治疗5年尚未发现对其耐药的CHB病例。
关于耐药监测,请见参考文献。
4.安全性:由于NAs主要从肾脏排泄,因此,在应用NAs前,应检测患者血清肌酐水平、计算肌酐清除率和估算肾小球滤过率(estmated glomerular filtration rate,eGFR),如肌酐清除率或eGFR<50 ml/min,则应调整NAs治疗剂量。此外,还应对失代偿期肝病、肝硬化、肌酐清除率< 60 ml/min、同时合并高血压、蛋白尿、糖尿病、活动性肾小球肾炎、实体器官移植等患者进行肾脏损害的风险评估。
NAs有可能导致肾功能下降。ADV连续使用4-5年,3%的患者出现肾毒性。有研究报道,ADV和TDF治疗可导致Fanconi综合征、肾功能不全、低磷性骨病和骨密度下降等。因此,对用ADV或TDF治疗的患者,应定期监测血肌酐并计算肌酐清除率、血磷和骨密度等。
GLOBE研究表明,接受LdT治疗2年的患者中,有3或4级肌酸激酶(CK)升高(>7倍正常值上限)者的比例为12.9%,并有2例出现有症状的肌病,如肌疼、肌无力等。Lai等报道,LdT治疗52周时CK升高率为7.5%(51/680),l例于LdT治疗Il个月后发生肌病。
我国任江波等报道,患者的CK升高率与其LdT治疗时间长短有关,治疗1年者为61.2%,治疗5年者为95.9%;CK升高的严重程度也与治疗时间长短有关,治疗1年时CK 3-4级升高率为4.1%,5年升至14.3%。因此,对接受LdT治疗的患者,应监测血清CK变化和横纹肌疾病的发生。
四、存在问题与未来研究课题
1.提高抗病毒药物的可及性:由于受药物价格、报销政策、认知水平及支付能力等因素的制约,我国仍有许多CHB患者未接受抗病毒治疗;已接受抗病毒治疗的患者,也有许多未采用国内外CHB管理共识或指南所推荐的高效低耐药抗病毒药物治疗。
因此,应通过政府部门、学术界、企业界和民间团体之间的良性互动,建立和完善药物审批及价格形成机制,充分发挥政府带量采购和报销政策对降低价格和优先选择药物的强大杠杆作用,以公共卫生策略来推动CHB的临床治疗,尽早实现政府、企业、患方和医方均受益的多赢结局。
2.制订行业规范,进一步提高我国CHB诊治水平:我国目前有相当一部分患者未按现行CHB管理共识或指南的建议进行规范的抗病毒治疗和定期随访。因此,应该充分发挥专业团体的学术引领作用和有关政府部门的规范管理功能,进一步加大对CHB管理共识或指南的宣传推广力度,并制订具有可操作性且有一定强制性的行业规范,提高我国CHB的诊治水平和整体卫生经济效益。
3.研究更可靠的NAs长期治疗CHB的停药标准和监测指标:国内外研究报道,即使按照现行的CHB管理共识或指南建议的标准停药,停药后的复发率仍高达50%-70%。因此,有必要研究NAs长期治疗CHB更可靠的停药标准和判断停药后复发与否的监测指标,如定量HBsAg水平和特异性免疫学指标等,将停药后复发率降至更低水平。
4.研究现有NAs更有效的长期治疗策略:有部分肝硬化患者经过长期治疗后发生了逆转,他们有可能停药;但还有相当一部分患者虽经长期治疗有所逆转,仍有严重的肝纤维化,可能需要终身治疗。对肝硬化患者的治疗策略值得进一步研究。
Ning等报道,应用ETV治疗达到病毒学抑制的CHB患者,改用聚乙二醇干扰素α-2a (PegIFNα-2a)治疗,可明显提高HBeAg血清学转换率和HBsAg消失率。但也有不同报道。至今关于NAs与PegIFN α联合或序贯治疗的研究还较少,尚需进行多中心随机对照研究证实。
5.研究NAs长期治疗的安全性:目前用于CHB治疗的NAs中,LAM已有16年历史,最后被批准上市的TDF也有7年临床应用历史。国内外临床研究表明,NAs是安全的。但更长时期的NAs单药或2种NAs联合治疗,以及特殊人群,如肝硬化失代偿、长期服用他汀类药物的患者等应用NAs长期治疗的安全性问题,有待进一步观察和评价。
参与讨论的专家(按姓氏拼音排序):
陈成伟、陈士俊、陈永平、成军、程明亮、窦晓光、段钟平、高志良、侯金林、贾继东、江家骥、李杰、李兰娟、李彤、鲁凤民、茅益民、缪晓辉、宁琴、牛俊奇、任红、孙永涛、谭德明、唐红、唐小平、万谟彬、王贵强、王豪、王慧芬、王宇明、魏来、翁心华、谢青、尤红、张文宏、张欣欣、庄辉
文章摘自《中华肝脏病杂志》2014年12月第22卷第12期P884